Gdzie w naturze występuje chlor?
Tak się składa, że najważniejszy związek chloru to chlorek sodu o wzorze NaCl, czyli sól kuchenna. Jest go mnóstwo w wodzie morskiej (dlatego jest słona). Występuje on również w złożach powstających na skutek wysychania mórz, które nie mają połączenia z oceanami. Z chlorku sodu uzyskuje się zarówno sam chlor, jak i jego związki. W pozostałościach po wyschniętej morskiej wodzie znajdziesz również inne związki chloru: sylwin (KCl, chlorek potasu), a także karnalit i kainit.
Chlor z punktu widzenia chemika
A teraz bardziej chemicznie. Chlor należy do grupy nazywanej halogenami (ewentualnie fluorowcami czy chlorowcami). W warunkach normalnych jest zielonożółtym gazem, który ma ostry charakterystyczny zapach i silnie podrażnia drogi oddechowe. A jakie są najważniejsze właściwości chloru? Podręczniki do chemii wymieniają te trzy:- duże powinowactwo elektronowe,
- wysoka reaktywność,
- silne właściwości utleniające.
Powinowactwo elektronowe
Mówiąc bardziej po ludzku… Czym jest powinowactwo elektronowe? Może pamiętasz, że atomy dążą do uzyskania na swojej ostatniej powłoce oktetu elektronowego*. Ponieważ halogeny znajdują się w 17 grupie, do pełni szczęścia brakuje im tylko jednego elektronu. Chlor bardzo chętnie przyjmuje dodatkowy elektron i przechodzi w jon ujemny (Cl–). Przyłączenie tego elektronu wiąże się z uwolnieniem energii.*Oczywiście wszystkie oprócz wodoru.
Powinowactwo elektronowe oznacza zdolność przyjęcia elektronu przez dany atom lub cząsteczkę. Im większe, tym chętniej atom/cząsteczka „przyjmuje” elektrony i tworzy anion.
Wysoka reaktywność chloru
Chlor jest bardzo aktywnym chemicznie pierwiastkiem. Gwałtownie łączy się z wieloma innymi pierwiastkami i związkami, i to już w temperaturze pokojowej. A co z cząsteczką gazowego chloru, czyli Cl2? Energia wiązania między dwa atomami chloru jest stosunkowo mała, więc łatwo ulega ono zerwaniu.Właściwości utleniające
Ta cecha chloru ściśle wiąże się z dwiema poprzednimi. Jest on świetnym utleniaczem.Utleniacz jest pierwiastkiem lub związkiem chemicznym, który w reakcji chemicznej przyjmuje elektrony i zmniejsza swój stopień utlenienia. Powoduje to, że inne pierwiastki lub związki chemiczne zwiększają stopień utlenienia.Oczywiście nic nie jest po prostu czarne albo białe. Więc, żeby nie było zbyt nudno, powiem ci, że w pewnych warunkach chlor może być również reduktorem. Taka ciekawostka! 🙂 Utleniacz i reduktor to pojęcia używane przy opisywaniu reakcji redoks. Jeśli do tej pory nie spotkałeś się z tego typu reakcjami i bilansem elektronowym, to głowa do góry – wszystko przed tobą 🙂 To jest cały dział w nauce chemii. Zdradzę ci tylko, że takie reakcje rozpisuje się na pojedyncze „procesy”, czy też akty utleniania i redukcji, czyli reakcje połówkowe. W ten sposób możesz mniej więcej sprawdzić, co się dzieje z danym związkiem lub pierwiastkiem – chociaż zazwyczaj mechanizm reakcji jest dużo bardziej złożony.
Jak chlor zachowuje się w wodzie?
Chlor dość dobrze rozpuszcza się w wodzie, tworząc wodę chlorową, używaną w laboratorium jako środek utleniający. Oprócz tego, że zachodzi proces fizyczny, chlor również powoli reaguje z cząsteczkami wody. W tej reakcji powstaje chlorowodór i kwas chlorowy (I) (dawniej znany jako kwas chlorawy) (patrz reakcja 1). Pod wpływem światła następuje rozkład tlenowego kwasu chloru (reakcja 2). Z tego względu wodę chlorową przechowuje się w butelkach z ciemnego szkła.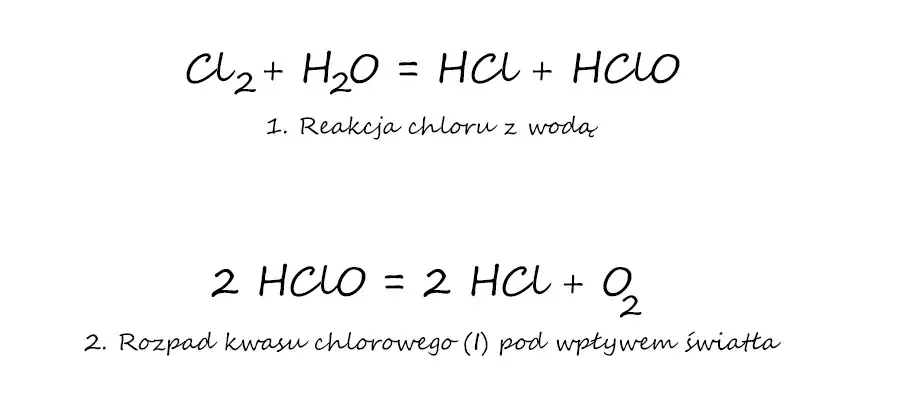 Ale rozpad kwasu cholorowego (I) to nie jest jedyny ciekawy „związek” między chlorem i światłem. Okazuje się, że..
Ale rozpad kwasu cholorowego (I) to nie jest jedyny ciekawy „związek” między chlorem i światłem. Okazuje się, że..
…chlor intensywnie „reaguje” na światło!
Za przykład niech posłuży reakcja powstawania chlorowodoru z gazowego chloru i wodoru. Jest to przykład łańcuchowej reakcji fotochemicznej. Najpierw warto jednak wyjaśnić, czym jest reakcja łańcucha oraz reakcja fotochemiczna.
Fotochemiczna reakcja łańcuchowa – co to znaczy?
Reakcja łańcuchowa na samym początku przebiega tylko w niewielkiej części ośrodka – czyli można to sobie wyobrazić, że w całym pokoju jedynie jedna cząsteczka chloru reaguje z jedną cząsteczką wodoru i powstają dwie cząsteczki chlorowodoru. To bardzo mała skala, prawda? Jednak pewne produkty tej reakcji (w tym wypadku reaktywne produkty pośrednie) inicjują kolejne reakcje, a potem kolejne i kolejne… I w tym momencie reakcja rozwija się lawinowo, bez potrzeby zewnętrznego czynnika inicjującego.Reakcja łańcuchowa na początku przebiega powoli, a potem jej szybkość gwałtownie rośnieReakcja fotochemiczna zachodzi pod wpływem promieniowania elektromagnetycznego, którego źródłem może być na przykład światło widzialne (tak jak w przypadku reakcji wodoru i chloru, którą będę omawiać). Cząsteczki substratu (albo substratów) pochłaniają kwant tego promieniowania, czyli foton (hv), który ma odpowiednią energię, żeby powstał wolny rodnik albo żeby substrat przeszedł w stan wzbudzony.
Reakcja fotochemiczna zachodzi m.in. pod wpływem światła widzialnego.
Reakcja wodoru z chlorem
W temperaturze pokojowej, w całkowitej ciemności, między gazami nie zachodzi żadna reakcja. Pod wpływem światła rozproszonego można zauważyć, że coś się dzieje, a w jasnym świetle słonecznym reakcja ma już przebieg wybuchowy.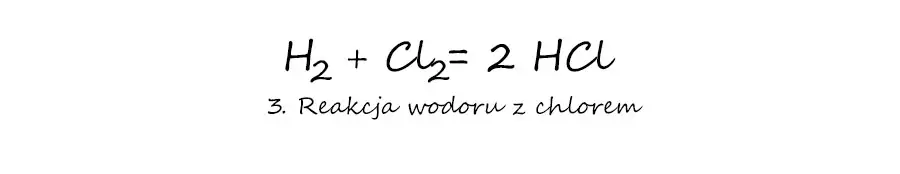 Wygląda niewinnie? Mechanizm tej reakcji można opisać następująco:
Wygląda niewinnie? Mechanizm tej reakcji można opisać następująco:
- Cząsteczka chloru pochłania dawkę energii i rozpada się na dwa niezwykle reaktywne rodniki (inicjacja łańcucha).
- Rodniki chloru reagują z cząsteczką wodoru – powstaje chlorowodór i rodnik wodoru. Z kolei rodnik wodoru reaguje z cząsteczkami chloru, przez co powstaje chlorowodór i kolejny rodnik chloru (rozwijanie łańcucha). Te dwie reakcje mogą się wielokrotnie powtarzać.
- W międzyczasie może zachodzić również reakcja przeciwna do powstawania chlorowodoru (inhibicja łańcucha). Rodnik wodoru może reagować z chlorowodorem, który już powstał, co daje nam cząsteczkę wodoru i rodnik chloru. Ta reakcja wpływa na na postęp sumarycznej reakcji (czyli nieco ją spowalnia), ale nie powoduje przerwania łańcucha – cały czas powstają bowiem nowe, aktywne rodniki chloru.
- Przerwanie łańcucha ma miejsce wtedy, gdy połączą się dwa rodniki (czyli wolne atomy) chloru. Jednak nie jest to takie proste – rozpędzone rodniki musiałyby jeszcze stracić część energii, żeby wiązanie między atomami nie uległo ponownemu rozpadowi wskutek drgań.

Zastosowania chloru i niektórych chlorków
Elementarny chlor stosuje się do wybielania oraz jako środek odkażający wodę (dlatego woda na basenie tak pachnie). Jest on również surowcem do produkcji związków chloru: chloranów (I), chloranów (V), tetrachlorku węgla czy chloroformu. Ma on również zastosowanie w niektórych przemysłowych syntezach związków organicznych. A co z chlorkami? Oto kilka przykładów. Chlorek potasu zastępuje chlorek sodu w przemyśle spożywczym. Chlorek cynku jest silnie higroskopijną substancją. Z tego względu jest wykorzystywany jako środek suszący. Ma on również zastosowanie w przemyśle (do oczyszczania powierzchni lutowanych czy przy wyrobie stopów cynku). Może być też mikronawozem, czyli produktem, który zapewnia roślinom jeden lub kilka mikroskładników. Właściwości higroskopijne ma również chlorek wapnia. Stosuje się go do osuszania gazów i ciekłych substancji organicznych. W duecie z chlorkiem sodu służy do posypywania jezdni zimą, w celu zapobiegania tworzenia się warstwy lodu. Ten związek chloru jest stosowany także w przemyśle spożywczym jako regulator kwasowości czy stabilizator.
Chlor – podsumowanie
Co już wiesz o chlorze?- To aktywny chemicznie pesymista (lubi „minusy” 🙂 ).
- Dobrze się czuje w wodzie – zarówno się w niej rozpuszcza, jak i z nią reaguje.
- Światło słoneczne dodaje mu „powera” w reakcji z wodorem w fazie gazowej.
- Ma różne zastosowania – zarówno „solo”, jak i „w związkach”.
A może masz ochotę dowiedzieć się czegoś więcej o innym halogenie – o jodzie? Zajrzyj do tego wpisu: Jod i jego właściwości (kliknij w tytuł lub obrazek poniżej).


